Ciencia
Bacterias resistentes
LA BIOINFORMÁTICA ACELERA EL HALLAZGO DE NUEVOS FÁRMACOS
jueves 23 de abril de 2026
Ante la crisis global de los antibióticos, un equipo científico de la UBA utiliza algoritmos avanzados para descubrir cómo atacar a las bacterias. Gracias a una plataforma desarrollada en Argentina y a la colaboración internacional, el equipo transforma la búsqueda de nuevos fármacos en un proceso eficiente que promete revolucionar la medicina moderna.
LA BIOINFORMÁTICA ACELERA EL HALLAZGO DE NUEVOS FÁRMACOS
Investigadores de la Universidad de Buenos Aires lideran una iniciativa que utiliza herramientas de inteligencia artificial para identificar los puntos débiles en bacterias resistentes a los fármacos actuales.
Mediante el análisis computacional de proteínas, el equipo logra identificar blancos moleculares con una precisión sin precedentes, transformando años de experimentación en el laboratorio en procesos digitales de alta velocidad que buscan soluciones soberanas a problemas de salud mundial.
Tras años de colaboración internacional, el equipo acaba de obtener un subsidio de la Fundación Gates para potenciar una plataforma propia que integra inteligencia artificial y modelos biológicos avanzados.
La tecnología permite reducir procesos que antes demandaban años a solo meses de trabajo computacional y validación dirigida. Esto permitirá pasar de testear millones de moléculas a solo un centenar con alta probabilidad de éxito. Ahora apuntan a una versión mejorada, que promete avances cruciales en la medicina, destacando el rol vital de la ciencia pública en Argentina.
La bioinformática contra las superbacterias
La resistencia de las bacterias a los antibióticos es un problema global, que la Organización Mundial de la Salud ha calificado como una prioridad urgente. Debido al abuso de los antibióticos, no sólo en humanos, sino por su uso en animales como pollos, cerdos y vacas, las bacterias han desarrollado tal resistencia que algunas de ellas ya no responden a los antibióticos tradicionales. Estas son las llamadas superbacterias.
En este contexto, Darío Fernández Do Porto, investigador UBA/CONICET en el Instituto de Cálculo de la Facultad de Ciencias Exactas y Naturales de la UBA, encabeza un esfuerzo innovador que se vale de la bioinformática para acelerar el descubrimiento de nuevas formas de combatir a la resistencia de las bacterias a los medicamentos convencionales.
"La bioinformática permite pasar de testear millones de moléculas a probar solo unas 100 con alta probabilidad de éxito", explicó Fernández Do Porto, subrayando cómo el lograr esta eficiencia resulta fundamental a nivel mundial, y en especial para sistemas científicos con recursos limitados, como el argentino.
Darío Fernándes Do Porto trabajando en la UBA.
El corazón del proyecto radica en la identificación de los llamados blancos moleculares, que son sitios específicos en las bacterias donde un fármaco puede actuar. Tradicionalmente, el descubrimiento de antibióticos era fortuito o basado en prueba y error. Como el caso de Alexander Fleming con la penicilina, donde un hongo contaminante reveló un "halo inhibitorio" contra bacterias. Hoy, con el auge de los datos genómicos y herramientas de inteligencia artificial, el enfoque es racional y predictivo.
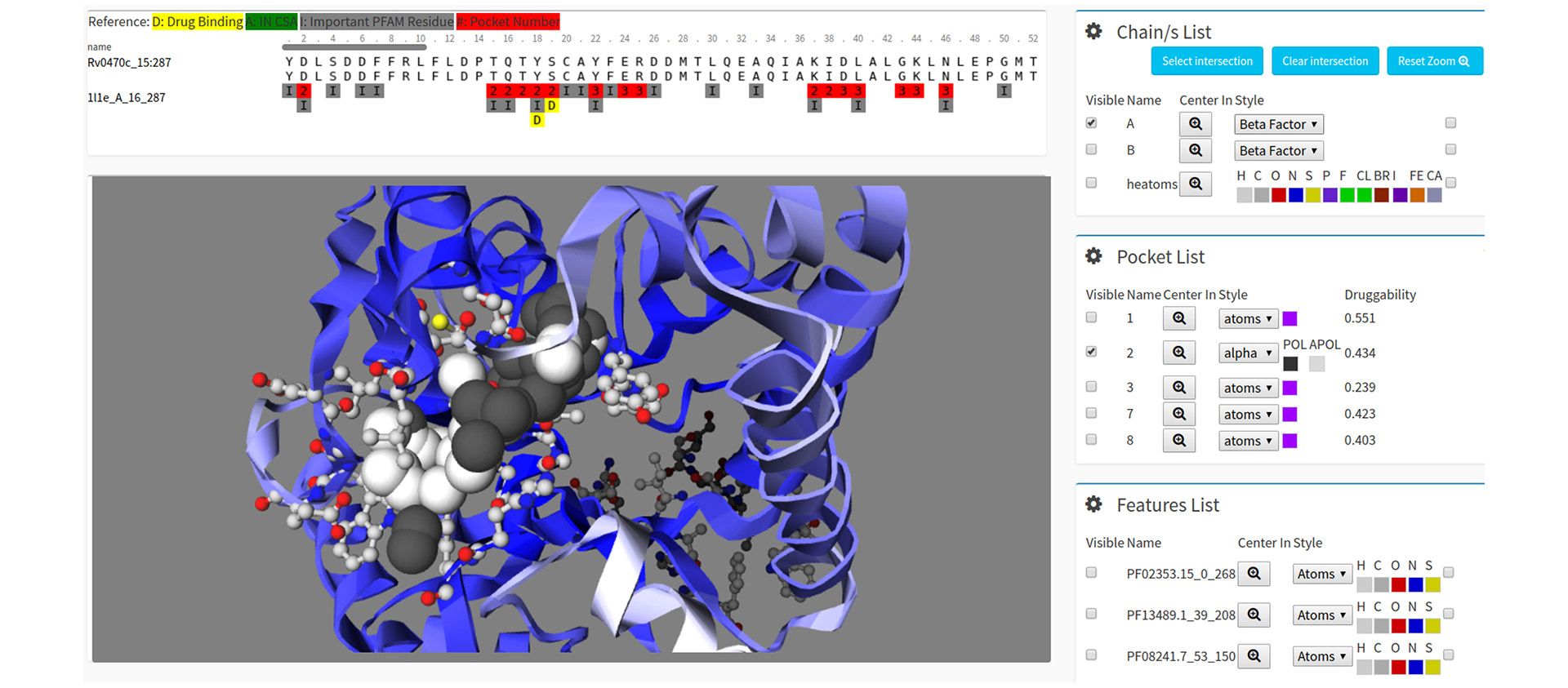
"Se toma el genoma de una bacteria, se predicen las estructuras de todas sus proteínas con el sistema de IA AlphaFold, y luego se usan algoritmos para identificar unas cavidades especiales, aquellas capaces de alojar un compuesto farmacológico", explicó Fernández Do Porto.
AlphaFold es una IA desarrollada por Google DeepMind que predice la estructura tridimensional de las proteínas con tal precisión que ha revolucionado la biología y la medicina. Tal fue el avance que se logró gracias a esta herramienta informática, que se le otorgó el Premio Nóbel de Química a sus desarrolladores.
Los algoritmos utilizados por el equipo de la UBA se entrenan haciéndoles ver miles de ejemplos de cavidades que unen drogas versus las que no, similar a cómo una IA distingue entre fotos de gatos y perros. El resultado se puede generalizar a todas las bacterias, si bien cada una, como la Klebsiella pneumoniae, tiene particularidades.
“Esta bacteria gram-negativa, resistente a múltiples antibióticos como los beta-lactámicos, los carbapenémicos y los polimixina, es uno de los focos principales del equipo debido a su alta mortalidad asociada a entornos hospitalarios”, contó el investigador.
En 2018, antes de la popularidad de la IA AlphaFold, el grupo de Fernández Do Porto desarrolló Target Pathogen, una plataforma web gratuita usada por investigadores de todo el mundo para buscar blancos a los cuales apuntar para luchar contra diversas bacterias.
Ahora, con un subsidio de la Fundación Gates, están creando la versión 2.0, incorporando IA para predecir blancos, así como también qué drogas –ya existentes o de diseño– podrían unirse a ellos.
"Podemos diseñar moléculas o seleccionarlas de bases de datos con millones de compuestos, y predecir si serán capaces de unirse a los blancos moleculares previamente seleccionados", afirmó Fernández Do Porto.
Esto invierte el proceso: primero el blanco, luego la droga, lo que acelera el desarrollo y reduce costos. En lugar de probar millones experimentalmente, la bioinformática filtra a un centenar enriquecido en candidatos prometedores, ahorrando tiempo, de meses a años, y mucho dinero, esencial en contextos como el argentino.
Colaboración internacional
El equipo sumó grupos de Uruguay, México, Portugal, Brasil, Chile y Canadá para postularse al subsidio de la Fundación Gates. De 800 proyectos que se presentaron de todo el mundo, lograron quedar entre los 21 finalistas, y ser elegidos para un subsidio.
“Venimos colaborando desde hace años con un equipo de Brasil, que lidera el proyecto financiado por la fundación Gates. Este equipo aisló en un hospital una cepa resistente a polimixinas y descifró su genoma. Publicamos trabajos en conjunto sobre blancos moleculares de posibles nuevos fármacoscapaces de potenciar la acción de este antibiótico. Desde la bioinformática seleccionamos pares blanco-compuesto, y el equipo de Canadá realiza la validación experimental en laboratorio”, explicó Fernández Do Porto.
Actualmente, tienen candidatos en una de las bacterias más preocupantes, Pseudomonas y planean extender a otra de las más peligrosas, que es Klebsiella. “Pero el camino hacia un fármaco viable es largo. De compuestos líderes a optimización, pruebas en laboratorio, patentes y, eventualmente, ensayos en animales y clínicos”, contó el investigador.
"El desarrollo de una droga cuesta en el orden de los mil millones de dólares", señaló, “pero la bioinformática reduce riesgos al proporcionar no solo candidatos, sino comprensión del mecanismo, crucial para reguladores como la FDA o ANMAT. Además, permite usar drogas existentes para nuevos fines, patentando su uso contra bacterias”.
Como biólogo con doctorado en química biológica y posdoctorado en bioinformática, Fernández destacó la importancia del factor humano, expertos en diferentes campos, junto a la IA.
"AlphaFold no triunfó únicamente por “fuerza bruta” computacional; fue clave incorporar biólogos para manejar el 'ruido' de los datos biológicos", contó. “La biología es dinámica, las bacterias mutan rápidamente bajo presión antibiótica, y la inteligencia artificial necesita del criterio experto para interpretar correctamente esa complejidad”.
El subsidio de la Fundación Gates valida la ciencia argentina, pero Fernández Do Porto advierte: "Llegamos aquí gracias a la universidad pública y fondos estatales. Sin inversión pública, no hay ciencia. La investigación científica y tecnológica, debe ser el motor de un país en desarrollo, con distribución de riqueza para devolver a la sociedad".
Este proyecto no solo combate superbacterias, sino que posiciona a Argentina en la vanguardia global. En un futuro incierto, donde infecciones resistentes podrían revertir avances médicos, iniciativas como esta ofrecen esperanza.
NOTICIAS RELACIONADAS:

DISEÑAN KIT DE DIAGNÓSTICO PARA CÁNCER DE PRÓSTATA CON AYUDA DE INTELIGENCIA ARTIFICIAL
martes 11 de febrero de 2025